临床研究
迈博药业作为领先的生物医药公司,专注于癌症和自身免疫性疾病的新药及生物类似药的研发和生产,拥有丰富的抗体药物储备。其候选药物管线包括多个单抗药物,其中部分已进入临床试验阶段,未来有望为更多患者提供新的治疗选择。
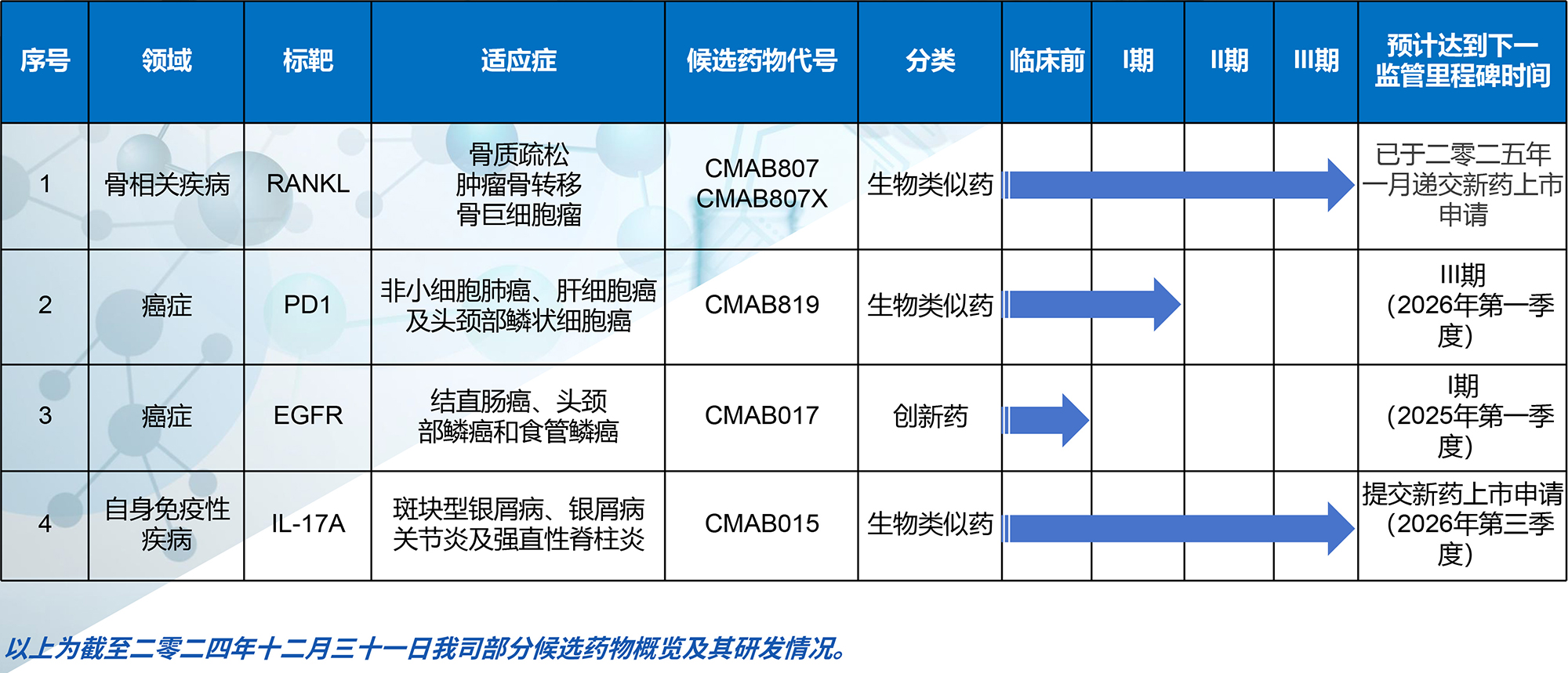
我们在加强现有上市药品生产制造的同时,公司仍在持续投入研发,推动新药的研发上市,以应对可能出现的药物短缺或新的疾病挑战。迈博药业正通过丰富的临床药品储备,为疾病治疗提供了更多选择,也为公共卫生安全提供了有力保障。
一种对人RANKL(核因子κB受体活化因子配体)具亲和性及特异性的人免疫球蛋白G2(IgG2)单克隆抗体,RANKL是破骨细胞(负责骨吸收的细胞)形成、发挥功能及存活所必需的跨膜或可溶性蛋白。CMAB807/CMAB807X阻止RANKL激活破骨细胞及其前体表面的受体RANK。阻止RANKL与RANK相互作用抑制破骨细胞的形成、发挥功能及存活,从而减少骨吸收并增加皮质骨及小梁骨的骨量和强度。
是可善挺®(司库奇尤单抗)的生物类似药候选药物。司库奇尤单抗是一种全人源单克隆IgG1 抗体,其主要作用机制在于选择性结合并抑制炎症通路中的关键因子白细胞介素17A(IL-17A),阻止其与白细胞介素17(IL-17)受体的结合,从而减轻炎症反应。这种药物的适应症包括中重度斑块型银屑病、银屑病关节炎和强直性脊柱炎。
为一种强抗体创新药物,CMAB017中,封闭肽的设计有望显著降低皮肤、消化道黏膜等的不良反应;人免疫球蛋白G1(IgG1)恒定区的选择可以增强抗体Fc段介导的效应,从而提高疗效。相比于已经上市的同类产品,CMAB017为疗效和安全性更佳的生物一类新药;且有望依托CMAB017的研发平台开发更多强抗体新药。CMAB017适用于治疗晚期实体瘤,包括但不限于结直肠癌、头颈部鳞癌和食管鳞癌。
为生物类似药候选药物。国家药监局已批准进行CMAB819 的临床试验。我们已经完成I 期临床试验。我们预期CMAB819 可能会于二零二八年第四季度获得国家药监局的上市批准。CMAB819适用于治疗转移性非小细胞肺癌、肝细胞癌及头颈部鳞癌。


